
国际泪膜与眼表学会(Tear Film&Oular Surface Society,TFOS)新版干眼症研讨会报告(Dry Eye Workshop,简称DEWS III)的发布,标志着干眼症诊断与治疗领域迈入新篇章[1]。干眼症在老年人群中尤为高发,一篇文献综述指出,40岁以上人群的干眼症患病率介于10%至20%之间[2]。
干眼症的诊断受多种因素影响,部分患者的不适症状可能由基础疾病引发,例如,约36%的干眼症患者合并睑板腺功能障碍[3];在出现睑缘炎症状的患者中,蠕形螨感染率介于29%至90%之间[4]。
美国北卡罗来纳州达勒姆市杜克大学Foster眼部炎症与免疫学中心主任Esen Akpek医学博士表示:“干燥综合征十分常见,在以水液缺乏为主要特征的干眼症患者中绝非个例。临床上,每10名症状明显的干眼症患者中,就有1人存在潜在的干燥综合征[5]。更值得关注的是,这些患者中超过半数在接受干眼症评估时,尽管已出现干眼症状且被诊断为干眼症长达10年,却尚未获得干燥综合征的官方医学诊断。”
无论干眼症症状与体征的诱因如何,专家强调,对患者进行全面诊断至关重要。下文将结合TFOS DEWS III报告内容,以及角膜病与干眼症领域临床医生的专业建议,详细梳理干眼症的诊断思路。
TFOS DEWS III的更新
2017年发布的TFOS DEWS II报告为干眼症的临床诊疗提供了指导,但随着干眼症相关研究的不断深入,临床医生的诊疗思路也在持续更新。最新发布的DEWS III报告整合了眼表疾病领域的最新数据与研究成果,旨在确保患者得到精准诊断[1]。该报告的核心更新包括“干眼症”定义的修订与诊断方法的优化。
一、干眼症的最新定义
当前定义明确:“干眼症是一种多因素引起的症状性疾病,核心特征为泪膜和/或眼表稳态失衡;其中,泪膜不稳定、泪液高渗透压、眼表炎症与损伤,以及神经感觉异常均为致病因素。”这一定义首次明确指出干眼症患者同时存在泪膜与眼表稳态失衡,而这一点在DEWS II报告中未被提及。
二、推荐的诊断方法与判定标准
表:OSDI-6问卷
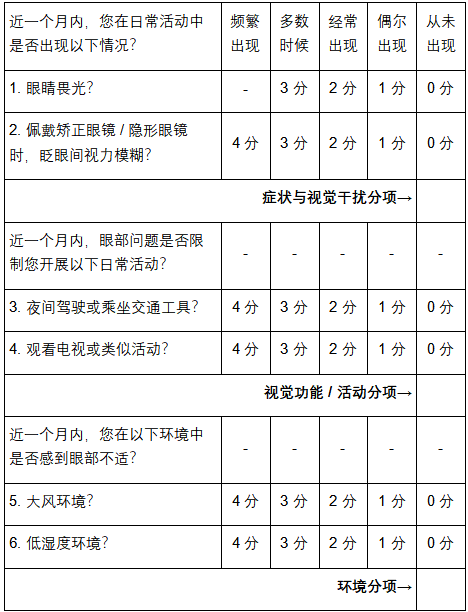
DEWS III报告提出,联合使用OSDI-6问卷(眼表疾病指数简化问卷)与非侵入性泪膜破裂时间检查或泪液渗透压检测,可显著提升诊断准确性。具体判定标准如下:
OSDI-6问卷:总分≥4分即可判定为干眼症阳性;
非侵入性泪膜破裂时间:检测值<10秒为阳性结果;
泪液渗透压检测:若任意一只眼的渗透压≥308 mOsm/L,或双眼渗透压差值>8 mOsm/L,即可诊断为干眼症。
使用活体染料诊断干眼症时,DEWS III推荐采用荧光素与丽丝胺绿对眼表进行染色,满足以下任一条件即可判定为干眼症阳性:
角膜荧光素点状染色>5个;和/或
结膜丽丝胺绿点状染色>9个;和/或
睑缘染色长度≥2mm且宽度≥25%。
三、干眼症亚型分类的更新
DEWS III报告还调整了干眼症的亚型分类方式,明确所有干眼症病例均存在蒸发过强成分,这与以往分类不同。此前,干眼症被简单划分为“水液缺乏型”与“蒸发过强型”,这种分类方式限制了临床治疗方案的选择。如今,通过对泪膜各层、眼睑及眼表进行检查,可进一步明确干眼症的严重程度与具体类型,进而指导治疗。
当前,干眼症主要按以下维度分类:
泪膜相关:脂质层异常、水液层异常、黏蛋白/糖萼层异常;
眼表及附属器相关:解剖结构异常、眨眼/眼睑闭合功能异常、睑缘异常、神经功能障碍、眼表细胞损伤/破坏,以及原发性炎症/氧化应激。
四、现有诊断方法的待改进方向
DEWS III报告作者指出,当前诊断方法仍需进一步完善,主要存在以下研究空白:
干眼症严重程度分级缺乏充足证据支持;
如何区分干眼症与过敏性眼病尚未明确;
未基于现有循证诊断阈值确定致病因素的判定标准;
评估眼表时,荧光素与丽丝胺绿的最佳染色顺序尚不明确。
深入问诊:挖掘症状根源
美国纽约威尔康奈尔医学院眼科医生Christopher Starr医学博士表示:“与其他眼病相比,眼表疾病的复杂性、诊疗难度与耗时程度都更高,因为这类疾病通常存在大量潜在诱因。想要充分了解患者病情,关键在于多提问、深入沟通,进而找到症状的根源。”
问卷虽能帮助初步了解干眼症患者的基本情况,但无法覆盖所有关键信息,例如环境因素、用药史及基础疾病等。因此,临床医生需通过与患者沟通,进一步明确干眼症的分型与严重程度。
Esen Akpek医学博士介绍:“我们诊所首先会让患者填写OSDI症状问卷,但在评估病情严重程度、患者生活质量受影响情况及用药依从性时,我还会针对性提问。例如,我总会问患者‘最困扰你的症状是什么’,有时最困扰患者的症状并非最常见的症状,这一点可能令人意外。比如,‘夜间驾驶’这一诱因可能严重影响部分患者的生活质量,但对另一部分患者则无任何影响。因此,了解每位患者的独特症状至关重要。”
她进一步解释:“OSDI是经过验证的标准化问卷,但主要评估症状出现的频率。DEWS III推荐使用更简洁、患者更易完成的OSDI-6简化版问卷,但从全面诊疗的角度出发,我认为OSDI-12(12项版)更实用,因此我们诊所采用的是OSDI-12。”
“由于最困扰患者的症状可能并非最常见症状,直接向患者询问这一点十分重要。对我而言,部分症状的临床意义更为关键:例如,视物模糊或视力波动、无法长时间阅读,可能提示角膜病变更严重;烧灼感/刺痛感不一定意味着水液缺乏性炎症型干眼症,但‘眼干感’则更能确诊水液缺乏性干眼症。水液缺乏性干眼症常与基础疾病相关,因此本质上属于炎症性疾病[6]。而睑板腺功能障碍虽常见,却不一定伴随炎症。”
正如DEWS III报告所强调,所有干眼症病例均存在蒸发过强成分,因此将患者简单归为“水液缺乏型”或“蒸发过强型”并无益处。临床医生建议通过更多提问,判断患者以哪种类型为主。
费城威尔斯眼科医院角膜科主任Christopher Rapuano医学博士表示:“若患者晨起时症状加重,可能提示病因与眼睑相关。根据我的临床经验,这种情况更可能与睑缘炎或睑板腺炎有关,因此我会重点询问患者是否有此类不适。”
“接下来,我会问患者‘哪些因素会加重或缓解你的症状’?有时,长时间驾驶、长时间使用电脑阅读等日常活动可能诱发症状,这类情况可能是蒸发过强型,也可能是水液缺乏型。随后我会追问‘什么方法能缓解眼干’?若患者回答‘滴眼药水后感觉很好,但效果很短暂’,我会进一步询问其使用过的药物:若患者仅使用过含防腐剂的眼药水,我就能找到部分症状的诱因;若患者已尝试过10种不同药物,说明病情更复杂,需要开展更多检查。”
Christopher Starr医学博士补充:“我总会询问诱发因素,比如过敏史,患者的症状是否在旅行或乘坐飞机后出现?是否在开始使用某种新药后出现?近期是否确诊皮肤病或自身免疫病?是否有病毒感染或其他身体损伤史?是否使用过新的眼部化妆品?是否有麦粒肿病史?是否使用过异维A酸?”
此外,部分眼表症状可能与干眼症表现相似(即“伪装症状”),因此详细了解患者的生活方式至关重要。若时间有限无法深入沟通,也可通过其他问卷辅助判断患者是否患有干眼症或其他眼表疾病。
Starr医学博士指出:“DEWS III推荐使用OSDI-6问卷,因其简便快捷、患者易完成。但我与美国白内障与屈光外科医师学会(ASCRS)角膜临床委员会共同设计的‘ASCRS术前SPEED II问卷’,不仅涵盖干眼症与睑板腺功能障碍,还包括其他眼表疾病亚型,并非像OSDI那样仅针对干眼症。该问卷也完全适用于非手术患者的日常诊疗。”
干眼症的相关检查
一、检查方法概述
目前已有多种检测干眼症体征的方法,但部分设备与检查项目成本较高。然而,拥有最新技术并不意味着能为患者提供精准诊断。专家表示,结合裂隙灯检查、眼表染色及其他检查项目,即可充分了解患者的干眼症病情,进而制定治疗方案。
Esen Akpek医学博士介绍了她常用的检查流程:“我常规开展的检查(按顺序)包括:泪液渗透压检测、未麻醉状态下的Schirmer试验以评估泪液分泌量;几分钟后,使用无防腐剂荧光素进行泪膜破裂时间检测,随后评估角膜染色评分。通常我会采用OSS评分系统(眼表染色评分)结合荧光素染色,辅助诊断干燥综合征,除非患者参与特定研究并要求使用指定评分系统。结膜丽丝胺绿染色是我开展的最后一项检查,染色评分可帮助评估患者眼表上皮损伤的范围与严重程度,若不进行活体染色,根本无法察觉损伤的真实程度。”
Christopher Rapuano医学博士的检查思路与此相似。尽管他近期未开展泪液渗透压检测(此前认为该检查操作繁琐、实用性有限),但目前市场上已出现ScoutPro(博士伦公司)、I-PEN(I-MED Pharma公司)等便捷有效的检测设备,因此DEWS III报告已将泪液渗透压检测列为推荐诊断方法。
Christopher Starr医学博士则认为,联合开展泪液渗透压检测、基质金属蛋白酶-9(MMP-9)检测与角膜知觉检测,可获取全面的客观数据。
二、重点检查项目详解
1、角膜知觉检测
Starr医学博士表示:“若患者出现眼表症状,技术人员会启动干眼症/眼表疾病检查流程,其中包括我认为至关重要的两项检查:泪液渗透压检测与MMP-9检测,技术人员会在我接诊前完成这些检查。近期,我还在眼表疾病患者的基础检查中加入了Brill角膜知觉计检测:这是一种非接触式工具,可在不破坏角膜完整性的前提下评估角膜知觉。技术人员在我进行裂隙灯检查前开展此项检测,不会影响眼表状态。该设备的独特之处在于,既能检测出角膜知觉减退(提示神经营养性角膜炎),也能发现角膜知觉过敏(提示可能存在神经病理性疼痛)。”
2、基质金属蛋白酶-9检测
基质金属蛋白酶-9(Matrix Metalloproteinase-9,MMP-9)是一种炎症标志物,可通过检测该酶辅助诊断干眼症及其他疾病。传统MMP-9检测需在实验室进行,但目前已有可在诊室开展的商用检测试剂盒(如QuidelOrtho公司的InflammaDry)。Starr医学博士表示,联合分析MMP-9检测与泪液渗透压检测结果,即可判断患者是否患有干眼症或其他眼表异常。
“例如,若患者MMP-9检测阳性但泪液渗透压正常,说明可能并非干眼症,需进一步寻找其他炎症来源,这可能涉及多种眼表问题;若两者均为阳性,提示可能是伴有明显炎症的干眼症;若泪液渗透压阳性但MMP-9阴性,则可能是蒸发过强型干眼症。这些组合结果可为临床决策提供依据。”
3、蠕形螨性睑缘炎检查
诊断蠕形螨性睑缘炎的经典方法是通过裂隙灯检查眼睑与睫毛,同时还能发现其他无需复杂技术即可识别的潜在体征。
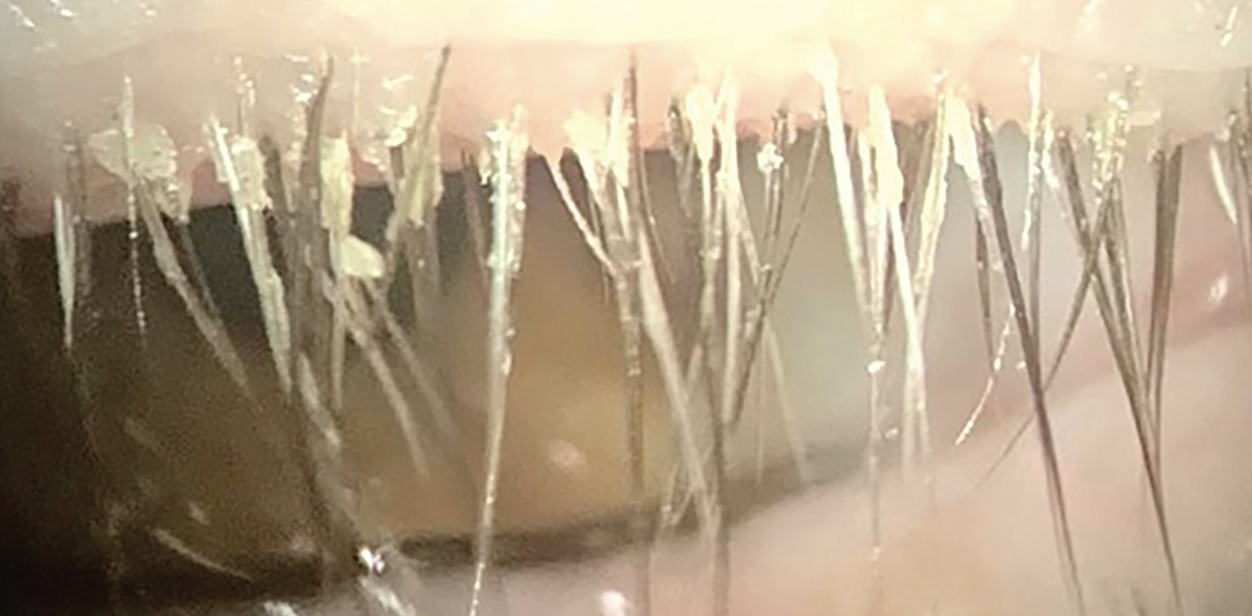
图注:怀疑存在蠕形螨性睑缘炎时,可在上睑缘睫毛根部观察到“袖套状鳞屑”。费城威尔斯眼科医院的Christopher Rapuano医学博士表示,在常规裂隙灯检查中,他会重点观察这一特征以明确干眼症病因
Rapuano医学博士介绍:“我的第一项检查是不使用任何眼药水、不进行染色的裂隙灯检查,首先观察眼睑与睫毛,初步判断患者前睑缘炎、睑板腺炎或后睑缘炎的严重程度。如今,我会重点观察‘袖套状鳞屑’——这是蠕形螨性睑缘炎的特征性表现。过去,由于缺乏有效的治疗方法,是否检出蠕形螨意义不大;但现在,这是我检查时首要关注的体征之一。”
4、结膜、泪河高度、翻转眼睑检查
Rapuano医学博士表示:“接下来,我会观察结膜,确认其外观是否正常、有无结膜瘢痕。部分老年患者可能出现结膜瘢痕,这有时是黏膜类天疱疮(又称眼瘢痕性类天疱疮)的早期表现。
“此外,我会在不滴任何眼药水的情况下观察泪河高度,判断泪液分泌是否充足。”
“我还会翻转眼睑检查睑结膜面,查看是否存在瘢痕组织。近期我接诊过一名患者,其睑结膜下存在钙沉积,这些沉积物全天摩擦眼球,导致眼部刺激症状,且药物治疗无效,患者的症状与干眼症十分相似,但病因实为钙沉积。此外,翻转眼睑还可能发现眼睑松弛综合征;若患者佩戴隐形眼镜,则可能观察到巨乳头性结膜炎。因此,对有干眼症症状的患者而言,翻转眼睑检查对排除‘伪装疾病’至关重要。”
5、眼表染色检查
眼表染色是诊断干眼症最常用的方法之一。联合使用荧光素与丽丝胺绿具有重要意义,因为这两种染料可针对性地显示眼表特定区域的病变,为判断干眼症病情提供关键信息。
Akpek医学博士解释:“使用角膜荧光素染色时,若在睑裂区中央或旁中央观察到点状上皮缺损,而角膜下方、上方或全角膜受累不明显,可能提示神经营养性角膜炎而非干眼症;根据染色模式,还可诊断隐形眼镜佩戴者是否存在角膜缘干细胞缺乏。此外,观察上方角膜缘角结膜炎需使用丽丝胺绿染色。这些检查并非干眼症的特异性检查,却有助于鉴别诊断其他眼表疾病。”
“结膜丽丝胺绿染色若在睑裂区鼻侧与颞侧呈现三角形分布,可辅助诊断干燥综合征,即便Schirmer试验结果正常,也需启动干燥综合征的相关检查。因此,密切关注所有检查结果的临床意义至关重要。”
6、睑板腺功能检查
由于干眼症患者常合并睑板腺功能障碍,因此需加入针对性检查。评估睑板腺功能的方法多样,部分患者希望通过直观数据了解病情变化,此时睑板腺成像设备可发挥重要作用。
Akpek医学博士表示:“我在诊所常规使用睑板腺成像设备,这项检查由技术人员操作,不会影响诊疗效率。该设备可帮助识别存在明显睑板腺功能障碍或睑板腺萎缩的患者,同时提供直观的图像资料,便于向患者解释病情并推荐门诊治疗方案。”目前常用的睑板腺成像设备包括iLux2(博士伦公司)、TearScience LipiScan(强生公司)与MeiboVue(VisuScience公司)。
对于没有睑板腺成像设备的临床医生而言,仅通过裂隙灯检查也可诊断睑板腺功能障碍,尽管这种方法无法为患者提供睑板腺的“可视化图像”,且评估睑板腺分泌物时可能引起患者不适,但依然有效。
Rapuano医学博士介绍了他的检查方法:“我会用棉签挤压睑板腺,观察分泌物(睑板腺脂质)的性状。正常的睑板腺脂质应如橄榄油般清澈,且挤压时易流出;若符合这一特征,说明睑板腺功能正常。”
“有时挤压睑板腺无脂质流出,这是异常表现;有时流出的脂质呈白色,同样异常;还有些时候会挤出牙膏状的白色分泌物,说明脂质已呈半固态,无法顺利排出以覆盖泪膜,这是严重睑板腺炎的表现。因此,检查睑缘、观察睑板腺开口,并通过挤压评估脂质性状至关重要,整个过程仅需10秒,操作简单且患者痛苦小(仅挤压眼睑时略有不适)。”
7、非侵入性泪膜破裂时间检查

图注:非侵入性泪膜破裂时间是TFOS DEWS III推荐的诊断测试之一,可使用市售设备进行,例如Oculus Keratograph 5M
DEWS III报告建议,可采用非侵入性泪膜破裂时间检查替代泪液渗透压检测。尽管并非所有诊所都配备Oculus Keratograph 5M或CSO Sirius+等非侵入性检测设备,但支持者认为,这些设备提供的数据与传统泪膜破裂时间检查同样有效,且可能提升患者满意度。
Akpek医学博士指出:“与使用活体染料的泪膜破裂时间检查相比,非侵入性检查无需滴眼药水,不会破坏泪膜稳态,因此具有优势。但目前很多诊所尚无可靠的非侵入性泪膜破裂时间检测设备。”
Starr医学博士也表示:“我目前无法开展非侵入性泪膜破裂时间检查(诊所无Oculus Keratograph设备),但我非常希望能开展这项检查,若有设备,我会对所有患者使用。我一直重视眼表疾病的客观数据,因此认为联合开展泪液渗透压检测、MMP-9检测、角膜知觉检测,以及(若可能)非侵入性泪膜破裂时间检查,才能真正全面了解每例干眼症患者的病情。我相信眼表疾病的诊断正朝着‘客观数据驱动’的方向发展,而这些检查工具能提供极具价值的数据。”
8、自动化干眼症检测设备
目前已有多种自动化干眼症检测设备可供选择:
Lacrydiag眼表分析仪(Lumibird Medical公司):符合DEWS II报告的诊断方法;
IDRA(SBM Sistemi公司)与OS1000(Reichert Technologies公司):两家公司合作推出的联合设备,可多维度评估眼表以诊断干眼症;
Tearcheck(ESW Vision公司):可评估眼表炎症、开展非侵入性泪膜破裂时间检查、提供睑板腺成像,并辅助检测蠕形螨。
Tera干眼成像仪(Topcon公司):这款多模态设备整合了OSDI-6患者问卷,可采集泪河高度、无创泪膜破裂时间、眨眼分析、脂质层参数、睑板腺成像、角膜地形图扫描、角膜波前数据、瞳孔测量结果、荧光素成像及眼前节摄影图像。通常情况下,要实现这些功能需使用多台不同设备。
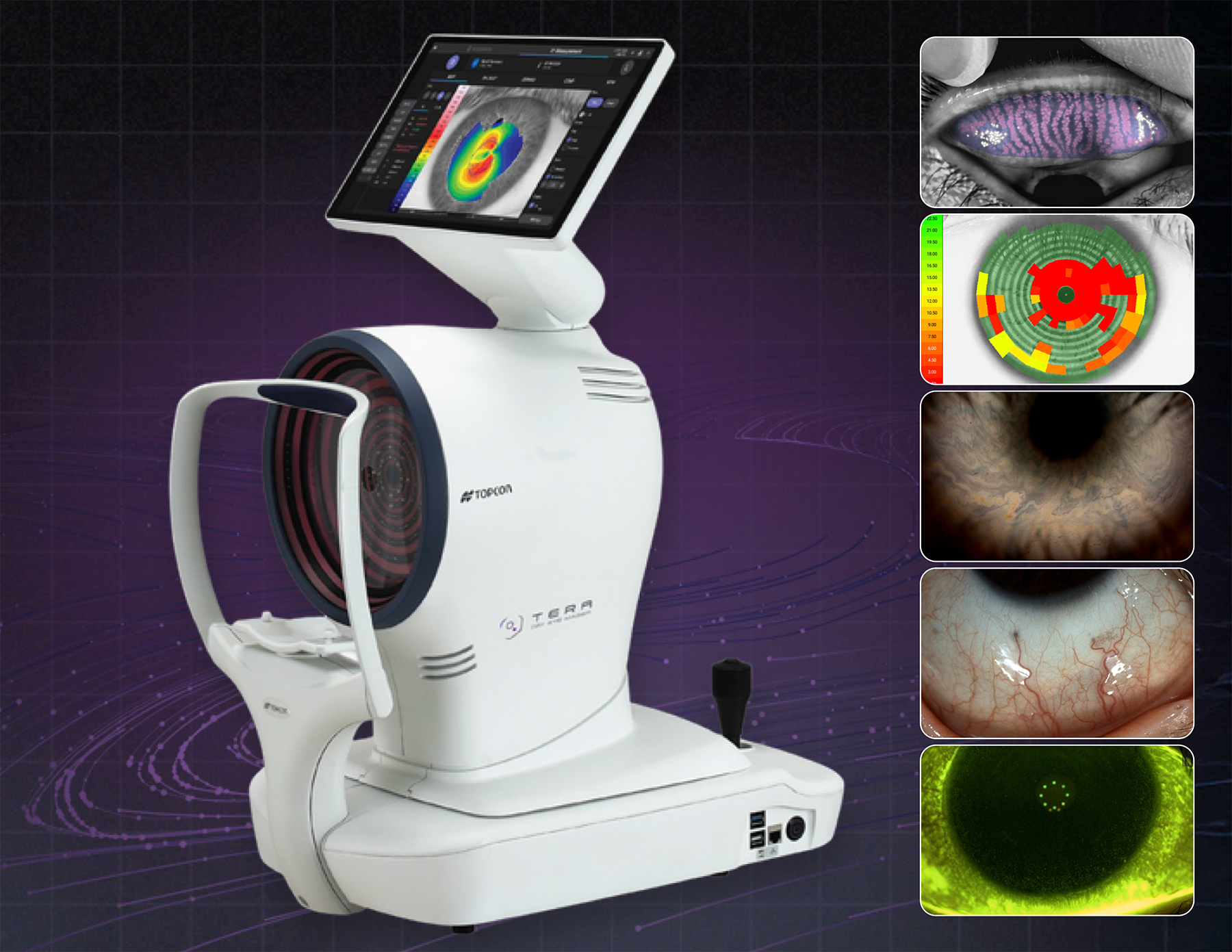
图注:Topcon Tera干眼成像仪
干眼症诊断的未来发展方向
Starr医学博士认为:“人工智能技术将成为辅助干眼症诊疗的重要工具。我认为AI永远无法取代临床医生,也无法替代裂隙灯检查与面对面诊疗,但眼表全天24小时暴露于环境中,而我们每年仅能为患者提供数次诊疗,获得的只是‘诊室快照式’的眼表状态数据,AI有望填补这一空白。”
DEWS III报告指出,机器学习技术有望提升干眼症诊断检查的客观性,但作者同时强调,AI诊断需以“疾病金标准组”为参照,才能提供可靠信息。因此,机器学习算法更适合用于收集与分层数据,为临床医生提供诊断指导。
“AI与可穿戴设备(如AI眼镜、智能戒指、智能手表)可在两次诊疗间隔期间收集大量有用数据,这些数据量庞大,可自动通过电子方式传输至电子病历(EMR)或相关软件。目前已有多家公司在研发这类技术,例如我担任顾问多年的CSI Dry Eye公司,就正尝试将此类功能整合到其软件中。”
具备AI功能的智能技术已能追踪日常健康数据多年,智能手机、智能手表、智能戒指与智能眼镜可收集体力活动(步数、卡路里)、心血管健康(静息心率、运动心率)与睡眠模式(时长、质量、睡眠阶段)等数据。这些数据有助于减少患者就诊时的问诊量。
干眼症诊断的有趣之处在于,临床医生的诊疗思路基本一致:部分医生可能会开展更多检查,但最终目标都是明确诊断。干眼症的诊断过程本质上是一系列“如果-那么”的逻辑判断:若患者回答X,则诊断为Y;若患者检查X阳性,则诊断为Y;若患者有症状但裂隙灯检查无异常,则需进一步检查以判断是干眼症、过敏性疾病还是其他眼表疾病。因此,花时间为每位患者收集全面信息,是确保干眼症精准诊断的关键。
TFOS DEWS III链接
一、TFOS DEWS III:社论
发布时间:2025年5月28日
链接:
https://www.ajo.com/article/S0002-9394(25)00273-9/fulltext

二、TFOS DEWS III:诊断方法
发布时间:2025年5月30日
链接:
https://www.ajo.com/article/S0002-9394(25)00275-2/fulltext

三、TFOS DEWS III:管理与治疗
发布时间:2025年6月2日
链接:
https://www.ajo.com/article/S0002-9394(25)00274-0/fulltext

四、TFOS DEWS III:摘要
发布时间:2025年6月3日链接:
https://www.ajo.com/article/S0002-9394(25)00276-4/fulltext

五、TFOS DEWS III:编者按
发布时间:2025年9月23日
链接:
https://www.ajo.com/article/S0002-9394(25)00516-1/abstract

六、TFOS DEWS III:执行摘要
发布时间:2025年9月24日
链接:
https://www.ajo.com/article/S0002-9394(25)00514-8/fulltext

参考文献:
[1] Wolffsohn JS, Benítez-Del-Castillo J, Loya-Garcia D, et al. TFOS DEWS III diagnostic methodology. Am J Ophthalm 2025; S0002-9394:25:00275-2.
[2] Britten-Jones AC, Wang MTM, Samuels I, et al. Epidemiology and risk factors of dry eye disease: Considerations for clinical management. Medicinia 2024;60:9:1458.
[3] Hassanzadeh S, Varmaghani M, Zarei-Ghanavanti S, et al. Global prevalence of meibomian gland dysfunction: A systematic review and meta-analysis. Ocul Immunol Inflamm 2021;29:1:66-75.
[4] Zhang AC, Muntz A, Wang MTM, et al. Ocular Demodex: A systematic review of the clinical literature. Ophthal Physiol Optics 2020;40:4:489-432.
[5] Akpek EK, Bunya VY, Saldanha IJ. Sjögren’s syndrome: More than just dry eye. Cornea 2019;38:5:658-661.
[6] Donthineni PR, Doctor MB, Shanbhag S, et al. Aqueous-deficient dry eye disease: Preferred practice pattern guidelines on clinical approach, diagnosis and management. Indian J Ophthalmol 2023;71:4:1332-1347.








