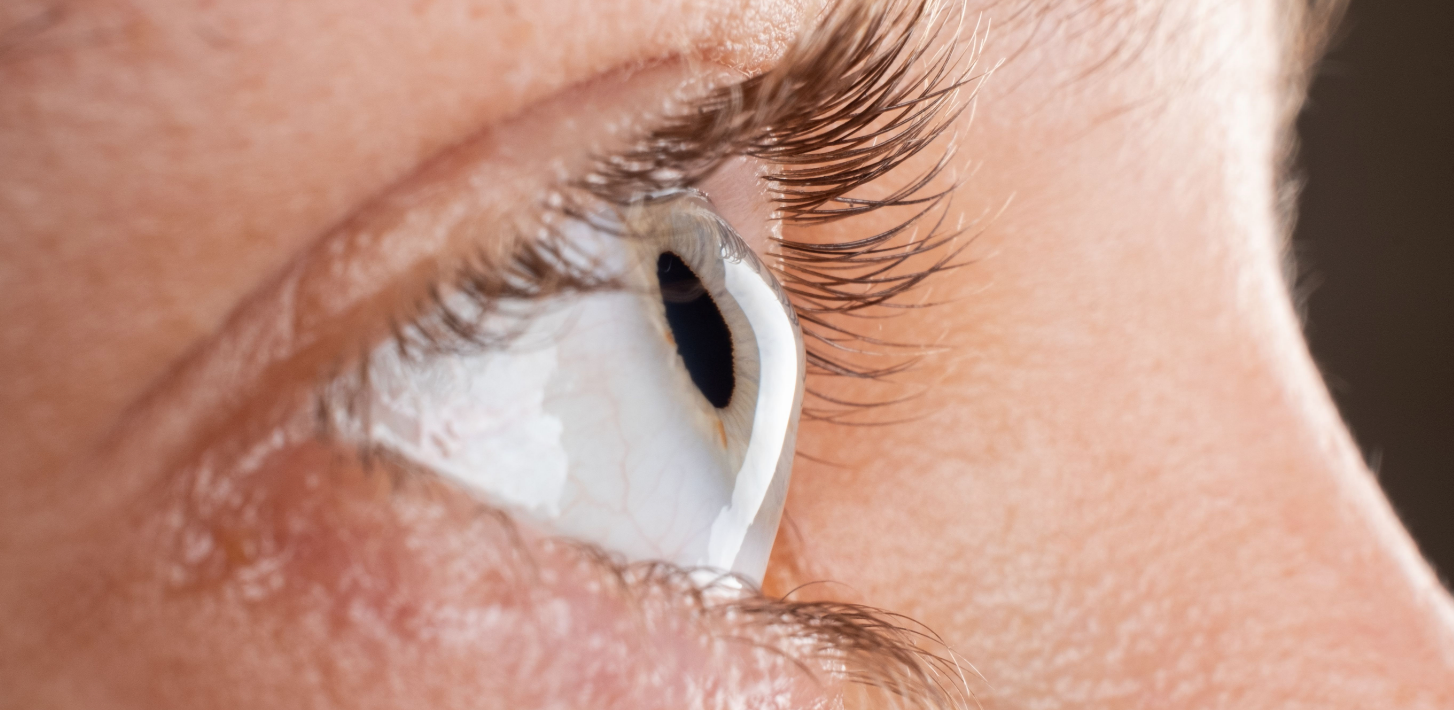
圆锥角膜(KC)作为一种进展性、可致盲的罕见眼部疾病,正困扰着全球超 2370 万患者,其中 30 岁以下人群的病情进展尤为迅猛。该疾病以角膜进行性变薄、变弱为核心特征,若未能及时干预,可能导致视功能丧失甚至失明,是美国穿透性角膜移植术的主要诱因之一。更严峻的是,圆锥角膜的漏诊与未治疗现象极为普遍,约 90% 的病例为双眼发病,未接受规范治疗的患者中高达 20% 最终需依赖角膜移植维持视力。长期以来,眼镜、隐形眼镜等传统手段仅能缓解视力症状,无法阻断疾病根本进展,临床亟需能兼顾疗效与安全性的创新疗法。
Glaukos 深耕眼科创新,Epioxa 突破交联术瓶颈
作为专注于青光眼、角膜疾病及视网膜疾病新型疗法的制药与医疗技术企业,Glaukos 始终以革新治疗标准为目标。公司曾率先推出微创青光眼手术(MIGS),并于 2012 年实现首款 MIGS 设备商业化;2024 年启动的 iDose® TR 作为首款长期作用的前房内手术用药物,为青光眼患者提供了 24 小时不间断的治疗方案。

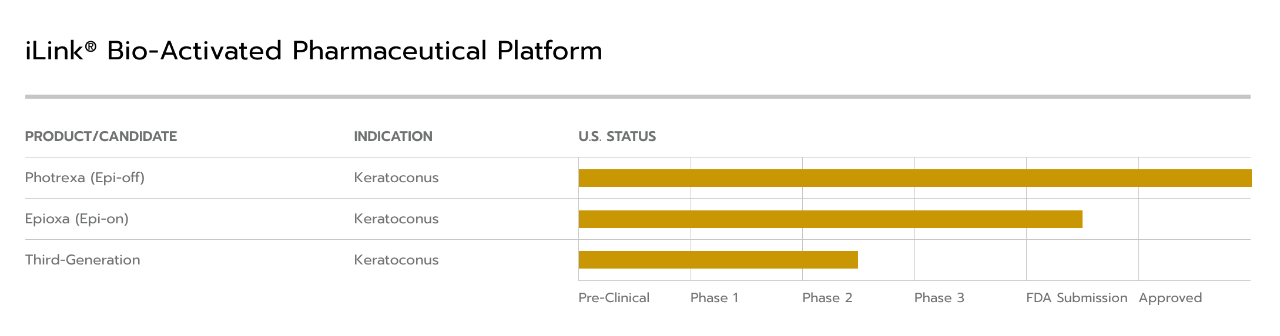
在角膜交联领域,Glaukos 同样积累了深厚的技术沉淀 ——2016 年获批的第一代 iLink 角膜交联疗法 Photrexa® Viscous/Photrexa®(上皮去除法,epi-off),作为首款经 FDA 批准的圆锥角膜治疗方案,其疗效与安全性已得到 300 余篇同行评审文献证实。
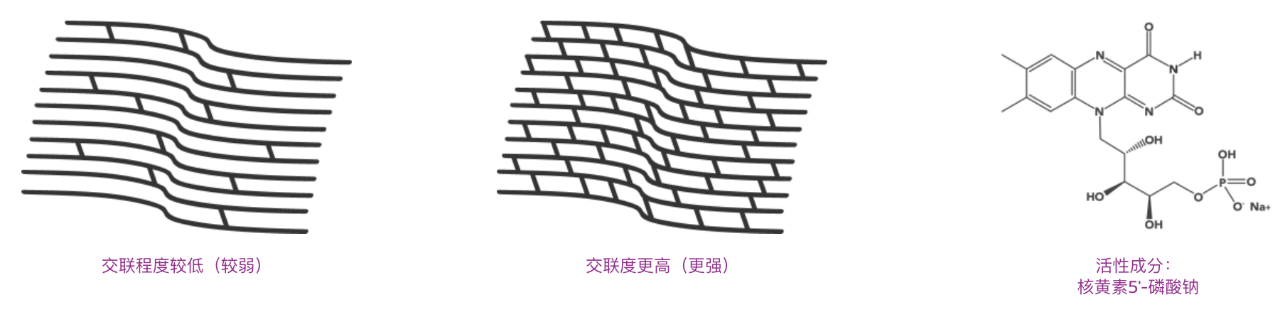
然而,传统上皮去除法存在显著局限:核黄素分子因体积过大无法穿透角膜上皮紧密连接,需先移除上皮才能实现角膜基质饱和,这一过程会导致患者术后疼痛、角膜混浊,且感染风险升高,需严密的术后药物管理。虽然后续出现的上皮在位法(epi-on)通过离子电渗疗法或渗透促进剂让核黄素穿透上皮,但受限于上皮对紫外线的吸收(约 20% 入射能量)及氧气扩散阻碍,交联效果往往欠佳。
针对这一痛点,Glaukos 通过创新技术组合实现关键突破:依托渗透促进剂、优化紫外线照射方案及大气氧气利用,其研发的上皮在位法角膜交联术已能达到与上皮去除法相当的角膜加固效果。2025 年 10 月 20 日,该公司第二款角膜管线产品 Epioxa™ HD/Epioxa™(简称 “Epioxa”)正式获 FDA 批准,成为首款且唯一经 FDA 批准、无需手术切口、无需移除角膜上皮的圆锥角膜局部药物疗法,标志着操作简便、效果确切的上皮在位法正式迈入临床应用阶段。
临床数据支撑安全疗效,多维度布局提升治疗可及性
Epioxa 的 FDA 批准基于两项前瞻性、随机、多中心、双盲 3 期关键性试验,共纳入 400 余名患者。试验结果显示,该疗法不仅达到了主要疗效目标,还展现出积极的安全性与耐受性。作为新型富氧局部治疗药物,Epioxa 经紫外线激活后,可彻底消除上皮移除带来的疼痛感,同时简化手术流程、缩短患者恢复时间,为患者、医疗服务提供者及医疗体系带来多重价值。其包含 Epioxa HD(0.239% 核黄素 5'- 磷酸眼用溶液)和 Epioxa(0.177% 核黄素 5'- 磷酸眼用溶液)两种制剂,需在交联手术中依次给药,并在富氧环境下通过紫外线激活,且仅可与 O2n™ 系统和 Boost Goggles® 配合使用。
从适应证来看,Epioxa 适用于成人及 13 岁及以上儿童患者的圆锥角膜上皮保留型角膜胶原交联治疗;禁忌症包括对产品成分(如苯扎氯铵)过敏者、无紫外线阻断人工晶状体的无晶状体眼和人工晶状体眼患者;有疱疹性角膜炎病史的患者需谨慎使用。临床数据显示,其最常见不良反应为结膜充血(发生率 31%),发生率 5%-25% 的不良反应包括角膜混浊、畏光、点状角膜炎、眼痛等,均在可控范围内。
Glaukos 董事长兼首席执行官 Thomas Burns 表示:“Epioxa 的获批为圆锥角膜患者建立了新的治疗标准,作为首款无需移除角膜上皮的 FDA 批准局部药物疗法,它显著提升了患者舒适度并缩短恢复时间,是该领域的创新性治疗方案。这一里程碑践行了公司‘改善患者获取保视疗法渠道’的使命。” 亚特兰大眼科顾问公司角膜专家、角膜学会主席 W. Barry Lee 医学博士也指出,漏诊、治疗不足以及传统手术的疼痛与漫长愈合期,是圆锥角膜患者治疗的主要障碍,而 Epioxa 无需切口、无需移除上皮的特性,恰好解决了这两大核心问题。
为解决圆锥角膜患者长期面临的漏诊与治疗不足问题,Glaukos 计划在患者认知与治疗可及性方面加大投入,覆盖疾病认知、诊断、治疗全流程:包括推出简化治疗获取的支持计划、降低经济负担的共付援助计划、面向医疗专业人员(HCP)与患者的综合教育策略,以及广泛的疾病认知与检测项目,推动早期筛查与诊断。预计 Epioxa 将于 2026 年第一季度正式商业化上市,为全球圆锥角膜患者带来全新治疗选择。








